a.銳鈦型晶種的制備
取一定量的清鈦液(控制過濾后未濃縮的鈦液),二氧化鈦含量約130~170g/L,三價鈦含量約2~5g/L,用濃度為100g/L左石的稀堿液(NaOH),在保持中和溫度不超過45℃,井、并有良好的攪拌情況下,緩慢發加入稀鈦液中進行中和,堿液加入的速度先快后慢,中和終點時的pH值為2~3,酸度系數0.26~0.30,TiO2濃度50~60g/L,在接近終點時要取樣預分析,如達不到上述指標可調整水、鈦液和堿的比例,然后用間接蒸汽在l0min內升溫至60℃,保溫30min進行酸溶熟化,生成藍色帶乳光的膠體晶種溶液,隨即急冷至室溫備用。
另一種銳鈦型晶種的制法是采用水解前的濃鈦液,用脫鹽水稀釋至30g/L,在攪拌下用濃度為100g/L的堿液(NaOH)中和,控制整個中和時間在30min內,先快后慢并保持中和溫度在60~65℃,中和終點pH為3.3~3.7, TiO2濃度為18~22g/L,然后急冷至30℃以下備用。該法的特點是中和時的溫度位于酸溶溫度區間,晶種的外觀渾濁不清,TiO2濃度較低。根據膠體化學的一般原理,當降低電解質濃度時,膠體溶液的穩定性增大,而且由于酸度的下降,晶種活性得到提高。但是晶種濃度過稀加量會太多,會降低水解起始時的鈦液濃度,因此該法主要適用于水解前要求鈦液濃度較高(215~230g/L)的外加晶種水解法,否則就不能保證200g/L的水解起始濃度。
最近有不少工廠采用一種稱為“快速晶種”的堿中和銳鈦型晶種。它的制法是在攪拌下把凈化后的鈦液一次性迅速加入80~100g/L的堿液中,保持中和期間的溫度在50℃以下,中和終點時的酸度系數在0.42~0.50之間,然后以2℃/min的速度升溫酸溶,但發現正鈦酸顆粒已明顯膠溶澄清時,保溫5min,接著再以2℃/min的速度升至70℃,保溫熟化15min后急冷備用。該法的特點是中和終點的酸度系數,不是在中和期間用試紙或酸度計測定,而是事先計算好鈦液和堿液的加量1次性加入,因此比較簡便、操作時還可以預留一部分脫鹽水在急冷時加到晶種中,既可做稀釋用水,又可幫助降溫。計算公式如下:
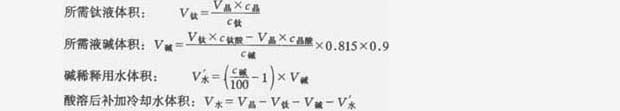
式中 v鈦——根據需要配制晶種量所需要的鈦液體積,L;
v晶——需要配制的晶種量,L;
c鈦——制備晶種用鈦液的TiO2濃度,g/L;
c晶——晶種濃度(按30g/L計);
v堿——所用堿液的體積,L;
c鈦酸—一制備晶種用鈦液的有效酸含量,g/L;
c晶酸——晶種有效酸含量(g/L,以0.48計);
c堿——已溶解好備用的堿液濃度,g/L;
v′水——把堿液稀釋至100g/L所需要的水量,L;
v水——酸溶后急冷時所需補加的冷卻水量,L;
0.815——酸堿中和常數(NNaOH/NH2SO4=40/49);
0.9——經驗常數。
這種晶種使用時可以在鈦液沸騰時加入。
b.金紅石型晶種的制備方法
并流晶種:在我國早期金紅石型鈦白粉生產中,曾廣泛使用過這種并流晶種。它的制備方法是將計算好的清鈦液和稀堿液(Na2CO3、NaOH),采用并流法中和,在整個中和期間保持pH3.8~4.5,然后水洗除去正鈦酸中的硫酸根離子,再用鹽酸加熱酸溶,使正鈦酸轉化成溶膠,當溶液變得透明轉而渾濁發生乳光時,停止加熱急冷后備用。這種晶種的活性較高,也比較穩定,但中和時pH控制很嚴格,正鈦酸水洗時很費時費事,如果硫酸根洗不凈,得到的是混晶型晶種,目前已很少采用。
四氯化鈦晶種:四氯化鈦晶種過去在國外采用的較多,該晶種的活性高,制備方法是先把四氯化鈦溶于水中,配制成475g/L的四氯化鈦溶液,另將氫氧化鈉配制成67g/L的堿液,把計算好的四氯化鈦溶液和堿液放入晶種制備罐中(搪瓷罐),在攪拌下進行局部中和,保留一部分過剩的鹽酸供酸溶時使用,中和溫度保持10℃以下,中和終點控制酸度系數為0.7~0.8(HCl/TiO2),然后在30min內升溫至80℃進行酸溶熟化,接著急冷至室溫后備用。該法因為四氯化鈦的貯存、運輸、稀釋時很麻煩,一旦泄漏會有大量氯化氫氣體溢出污染環境,國內很少采用。
煅燒晶種:煅燒晶種又稱二次晶種,是目前普遍使用的一種金紅石型晶種。前面兩種金紅石型晶種,屬于水解晶種(在水解時加入),現代金紅石型鈦白粉生產中,水解時不需要添加金紅石型水解晶種,而是采用普通的銳鈦型水解晶種,然后在漂白或鹽處理時加入煅燒晶種,因此又稱二次晶種。
煅燒晶種的制法大致為將漂白水洗合格后的偏鈦酸與堿(NaOH)在高溫下煮沸堿溶,兩者的比例為NaOH:H2TiO3=2.3:1,偏鈦酸的漿液濃度≥300g/L,堿液濃度≥42%,堿溶溫度為110~115℃,保沸4h,使偏鈦酸生成偏鈦酸鈉,反應式如下:
H2TiO3+2NaOH→Na2TiO3+2H2O
反應物在夾套冷卻水的冷卻下,于60℃放入水洗罐,主要洗掉游離堿和硫酸根,除去鈉離子和硫酸根能提高晶種的活性,偏鈦酸鈉在水洗時有部分會水解生成正鈦酸。
然后用鹽酸中和至pH3.5,使所有Na2TiO3生成H4TiO4沉淀下來。
接著把沉淀物再水洗2次,洗去氯根后進行酸溶,酸溶溫度110℃,保沸2h后急冷至40℃備用。制得的煅燒晶種濃度60~70g/L,金紅石型轉化率98%~100%,電鏡照片晶種呈良好分散狀態的柳葉形顆粒,煅燒晶種的加量一般為2.5%~5%。
用四氯化鈦也能制備煅燒晶種,它比用偏鈦酸制成的煅燒晶種在煅燒時晶型轉化的溫度更低,但操作復雜,四氯化鈦采購運輸比較困難,用偏鈦酸為原料,可以直接使用生產中的半成品來制備比較方便。
(4)制備晶種時的注意事項
a.中和操作
硫酸氧鈦與氫氧化鈉的中和反應是一個放熱反應,因此要控制加堿的速度和時間,避免中和時溫度過高局部發生硫酸氧和正鈦酸熱水解生成偏鈦酸而降低晶種的活性,反應式如下:
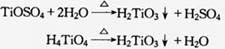
但是中和溫度也不能過低(低于30℃),過低會影響堿的分散使反應不均勻,甚至局部發生過中和而降低產品質量。因為當中和過量時,鈦液中的鐵會生成氫氧化鐵沉淀而污染產品,反應式如下:
FeSO4+2NaOH→Fe(OH)2↓+Na2SO4
因此中和終點時的pH一般不超過4,相反如果中和度不足,會使生成的晶種中晶核數量減少,會在水解時由于結晶中心數量不足造成水解率降低,水解顆粒細而難水洗。
中和終點時的pH高低直接影響酸溶時的溫度和時間,當中和pH值低時,正鈦酸的沉淀在酸性介質中完成,部分TiO22+呈游離狀態吸附在沉淀物的表面,帶有正電荷,酸溶時消耗的鹽酸也少,晶種穩定性好。如果中和時pH過高,沉淀物在中性(pH=7)條件下完成,其顆粒不帶電,TiO22+離子會與OH-離子結合,使溶液中不存在TiO22+,晶種穩定性低、活性差,酸溶時消耗的鹽酸也多。
大多數的情況下,中和時都是采用把堿加到鈦液中的方式,因為當鈦液做為分散相時,可以避免鈦液中的鐵進入晶格中。中和時的攪拌速度也很重要,一般控制在60r/min左右,過于激烈的攪拌會降低晶種的穩定性。
b.酸溶操作
中和所生成的正鈦酸沉淀是無定型的分散體,只有經過酸溶才能生成銳鈦型或金紅石型晶種。未酸溶的正鈦酸有被鈦液中的游離酸溶解的傾向,而且存放時間過長有改變其結構的危險,通過加熱酸溶熟化使膠粒微晶化,生成不溶于稀酸的膠體顆粒,并不能用普通的過濾方法使它分離,此膠體溶液帶有輕微的乳光而不發生沉淀,操作時可以從乳光的出現來判斷酸溶的終點。
酸溶的溫度與酸溶的時間有一定的依存關系,一般溫度高、時間短;溫度低則時間長。由于晶種的熱穩定性比鈦液還要差,故酸溶時的溫度不能高,時間也不能長,過高的溫度和過長的時間都會引起晶種的水解而降低活性。
酸溶后的急冷是很重要的,因為在此溫度下的膠體二氧化鈦含量最高,同時也極不穩定,必須迅速冷卻后才能保證它的活性和穩定性。
當用一價陰離子的強酸(HCl、HNO3、HF等)來酸溶時,水合二氧化鈦吸附一價陰離子,因一價陰離子的半徑較小,不會阻礙銳鈦型的微晶向金紅石晶型轉化,所以制得的是金紅石型晶種。而二價以上的陰離子(SO42-、PO43-等)會阻礙銳鈦型向金紅石型轉化,在制備銳鈦型晶種時,酸溶時使用的酸是鈦液中的有效酸(H2SO4),因此制得的晶種是銳鈦型。
C.成品晶種的濃度
許多研究資料都證明晶種中膠體二氧化鈦含量的多少是晶種活性高低的主要標志,但是晶種中膠體二氧化鈦含量越高越不穩定,試驗證明當晶種二氧化鈦濃度為84.8g/L時,存放72h即發生渾濁,當晶種濃度稀釋1倍(42.4g/L)后,放置148h后才產生渾濁。但是晶種濃度太低會沖淡水解鈦液的濃度,一般金紅石型晶種的TiO2濃度偏高,可以使水解時水合二氧化鈦的粒子較細,對產品的消色力、遮蓋力等有好處,而銳鈦型晶種因為它本身的結晶中心較細,故不必再提高它的濃度。并流法晶種之所以穩定性好,是因為它的正鈦酸在酸溶前要經過洗滌,正鈦酸的純度比較高所以穩定性好。
晶種的質量主要取決于晶種的活性、穩定性和膠粒的均勻程度,目前還沒有比較好的分析方法。有人用電位滴定法來測定聚合離子的多少和聚合度的高低來表示溶液中活性二氧化鈦含量的高低;有人認為晶種在水解時的結晶中心靠羥橋(OH-)和氧橋(O2-)來誘導水解,因此可以用測定羥絡基的含量或羥絡基團和氧絡基團的比值[(OH-)/(TiO22+)]來表示晶種的活性高低,但是以上方法在工業生產中都未正式采納,唯一確保晶種質量的辦法,就是按工藝要求認真一絲不茍地操作。
d.晶種的貯存
一次晶種(水解晶種)穩定性都不太好,一般只能存放24h,所以工廠操作時都是現配現用,最好1次用完,也不允許用不完剩余的部分與下一批晶種混在一起用,而二次晶種(煅燒晶種)穩定性較好,可以長期存放不變質。
